政策法规 || 《模型引导的创新药物剂量探索和优化技术指导原则》(附法规概览12.23-1.3)
01
国家药监局药审中心关于发布《模型引导的创新药物剂量探索和优化技术指导原则》的通告(2024年第53号)
为推动创新药物高质量发展,进一步指导我国创新药物临床试验阶段剂量探索和优化,药审中心组织制定了《模型引导的创新药物剂量探索和优化技术指导原则》(见附件)。根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查同意,现予发布,自发布之日起施行。

扫描图中二维码
查看详细信息

02
国家药监局关于发布《药品生产质量管理规范(2010年修订)》药用辅料附录、药包材附录的公告(2025年第1号)
为贯彻落实《中华人民共和国药品管理法》《中华人民共和国药品管理法实施条例》《药品注册管理办法》《药品生产监督管理办法》等有关规定,监督指导药用辅料、药包材生产企业规范生产,国家药监局根据《药品生产质量管理规范(2010年修订)》第三百一十条规定,组织制定了药用辅料附录、药包材附录,作为《药品生产质量管理规范(2010年修订)》的配套文件,现予以发布(见附件1、2),并就加强药用辅料、药包材质量监管有关事项公告如下:

扫描图中二维码
查看详细信息

03
关于公开征求《化学仿制药参比制剂目录(第九十批)》(征求意见稿)意见的通知

扫描图中二维码
查看详细信息

04
关于发布《国家药用辅料标准编写细则(2025年版)》的通知
扫描图中二维码
查看详细信息

01
截止2025年1月3日17:00本周发布210个待领取药品批准证明文件,其中注射剂67个,一致性评价品种9个。
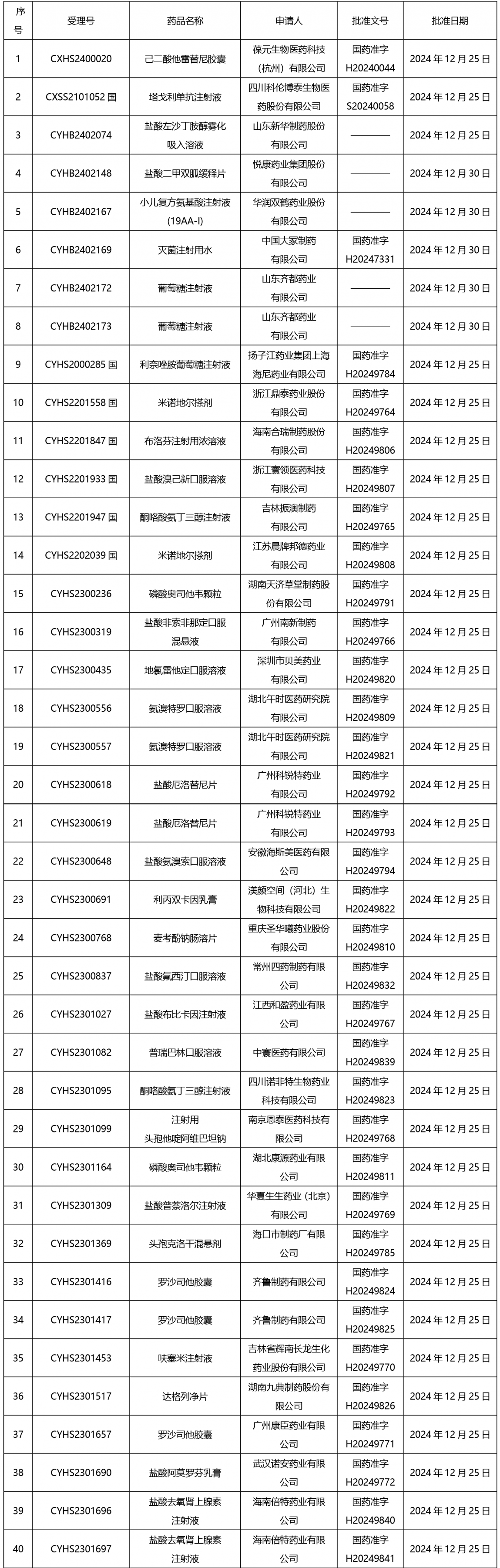
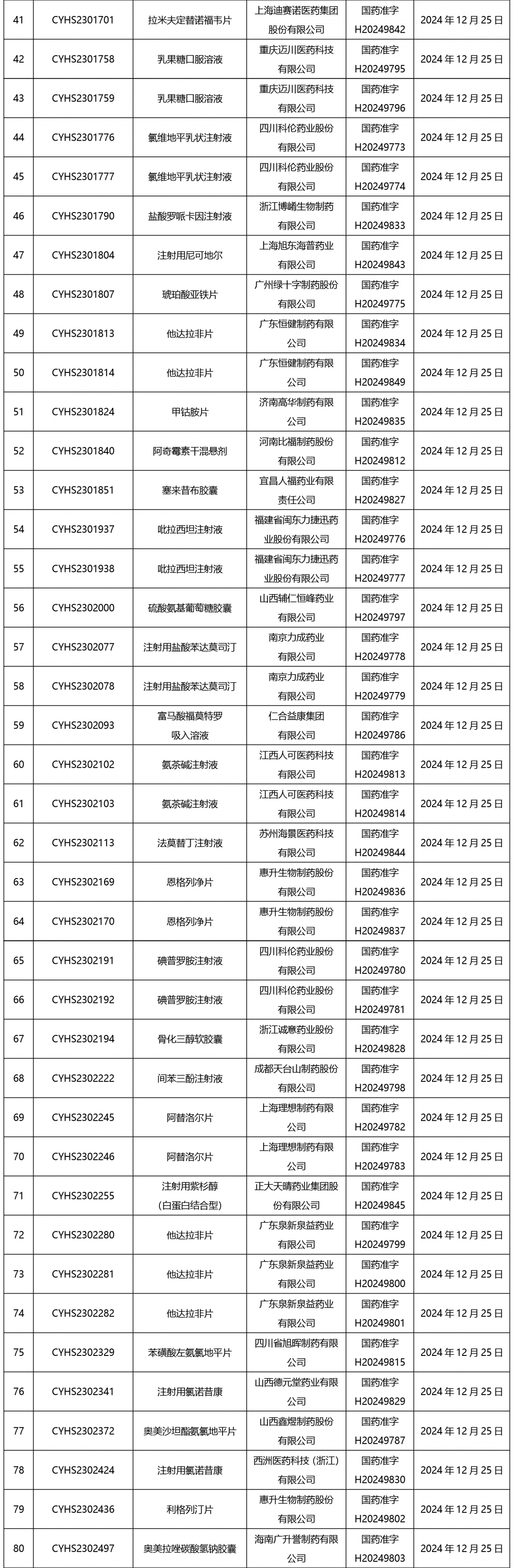
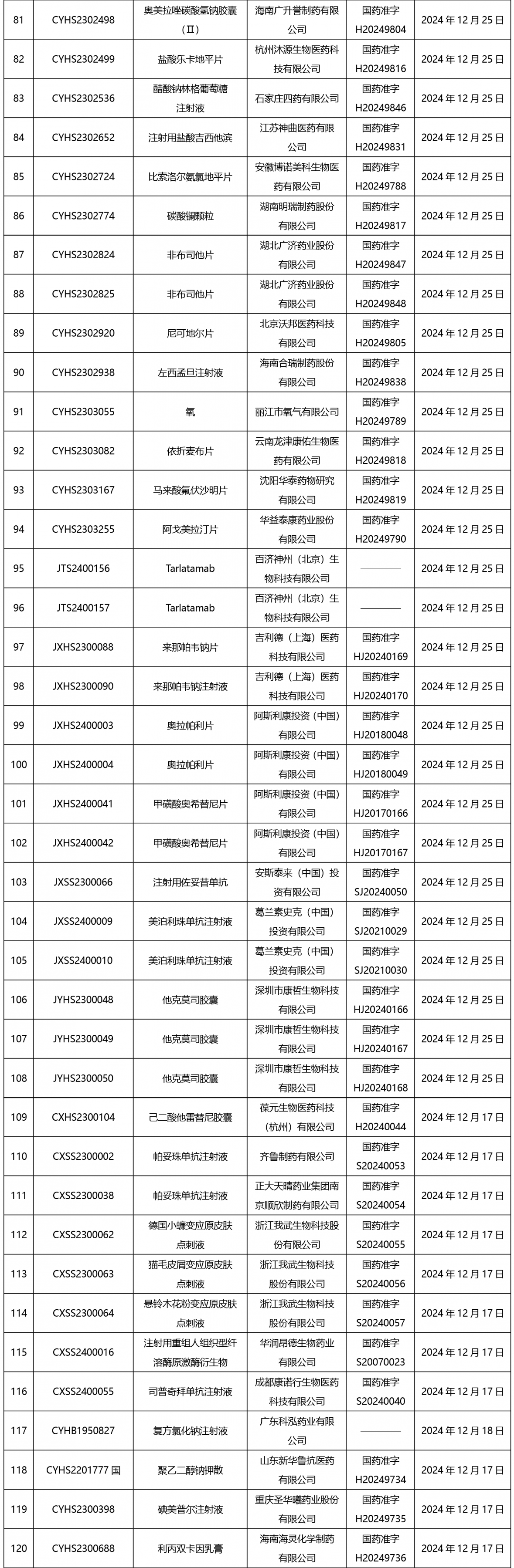
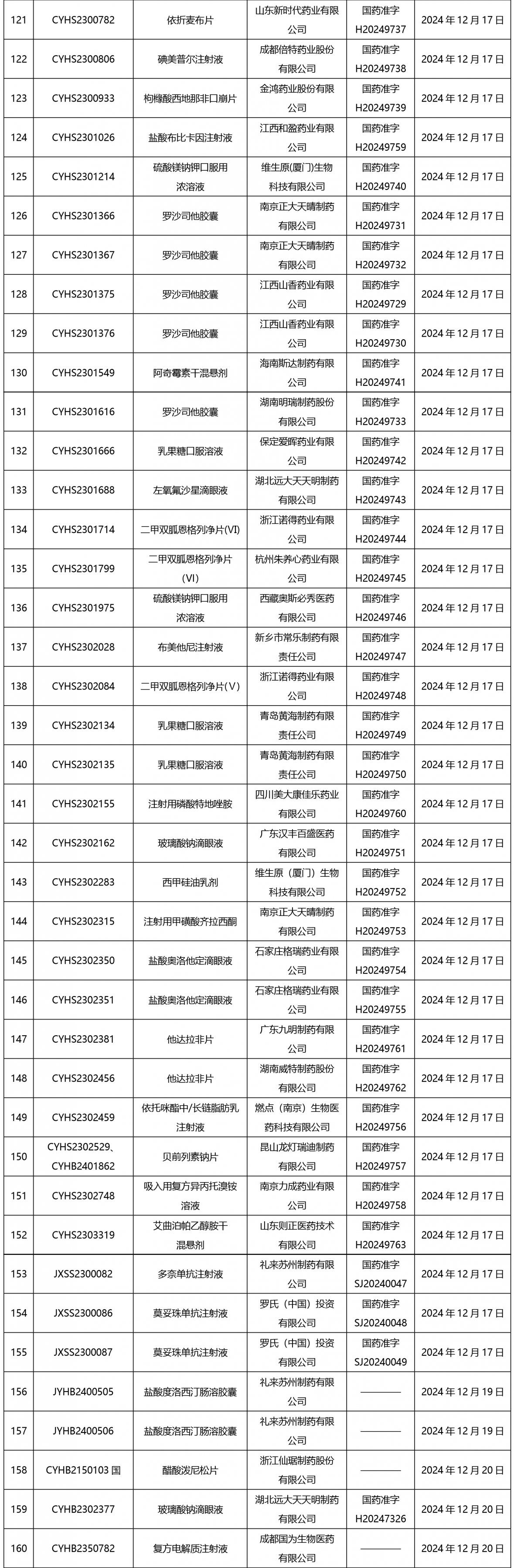
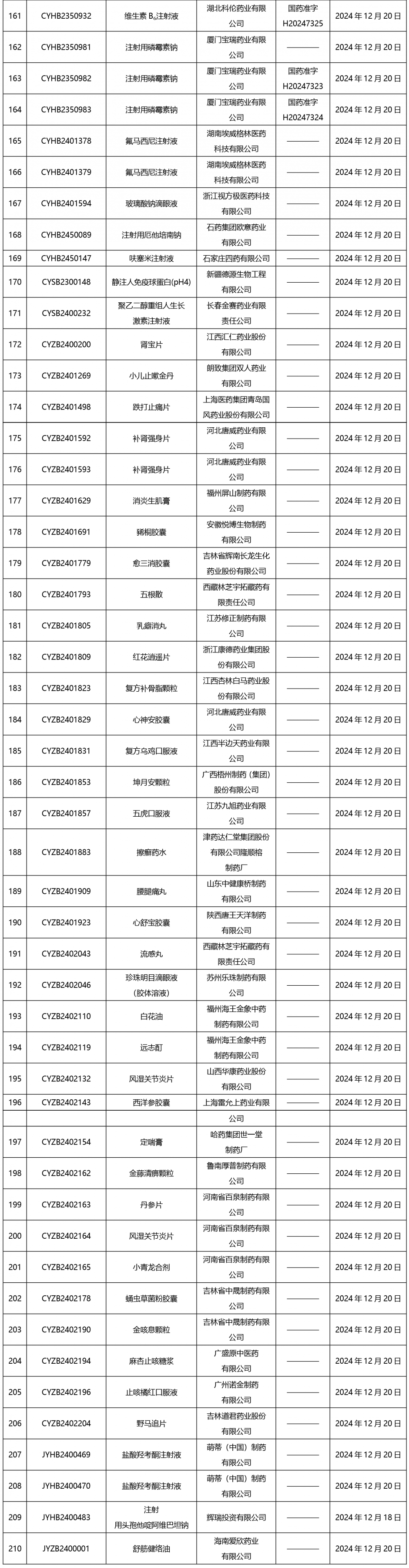
02
国家药监局关于枸橼酸铋钾颗粒处方药转换为非处方药的公告(2024年第155号)

扫描图中二维码
查看详细信息

03
国家药监局关于注销颠茄磺苄啶片药品注册证书的公告(2025年第2号)

扫描图中二维码
查看详细信息

01
关于公开征求《简化港澳已上市传统口服中成药内地上市注册审批申报资料及技术要求(征求意见稿)》意见的通知

扫描图中二维码
查看详细信息

02
国家药监局药审中心关于发布《评价胰岛素类药物药代和药效动力学的正葡萄糖钳夹试验指导原则》的通告(2024年第56号)

扫描图中二维码
查看详细信息

03
国家药监局药审中心关于发布《肽类药物临床药理学研究技术指导原则》和《抗体类药物临床药理学研究技术指导原则》的通告(2024年第55号)

扫描图中二维码
查看详细信息

04
国家药监局药审中心关于发布《多糖结合疫苗药学研究及评价技术指导原则(试行)》的通告(2024年第51号)

扫描图中二维码
查看详细信息

05
国家药监局药审中心关于发布《疫苗临床试验统计学指导原则(试行)》的通告(2024年第52号)

扫描图中二维码
查看详细信息

06
国家药监局药审中心关于发布《药物临床试验样本量估计指导原则(试行)》的通告(2024年第54号)

扫描图中二维码
查看详细信息

01
关于药品注册申请人之窗联通政务服务门户的通知
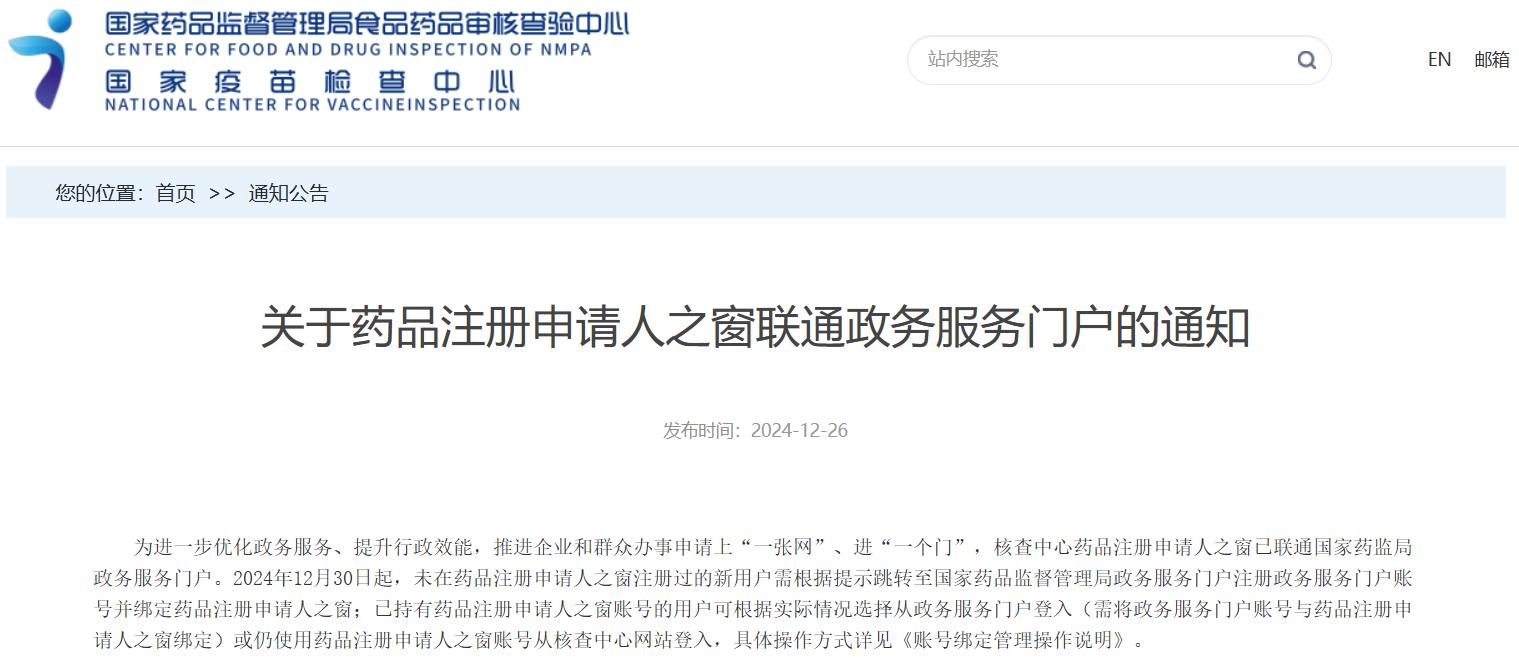
扫描图中二维码
查看详细信息

近期,药典委发布的标准草案公示如下:
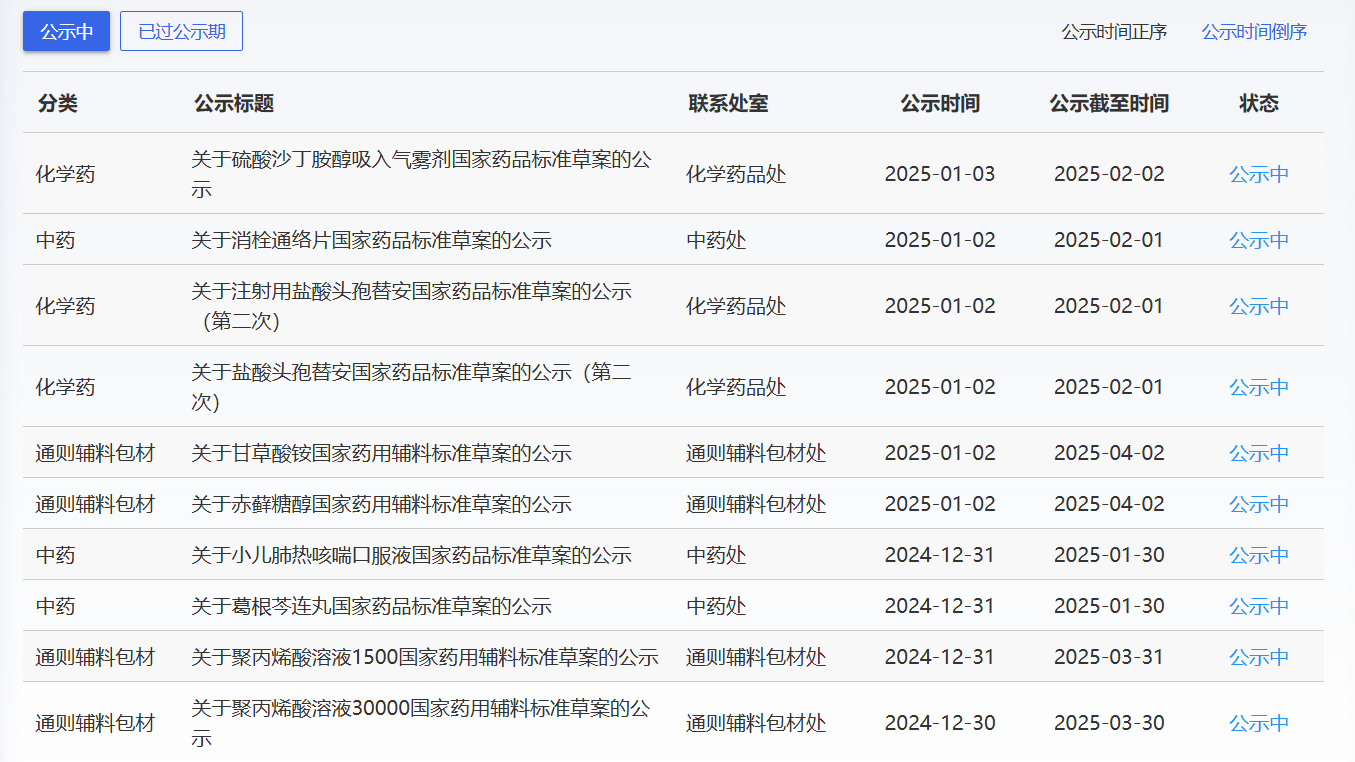
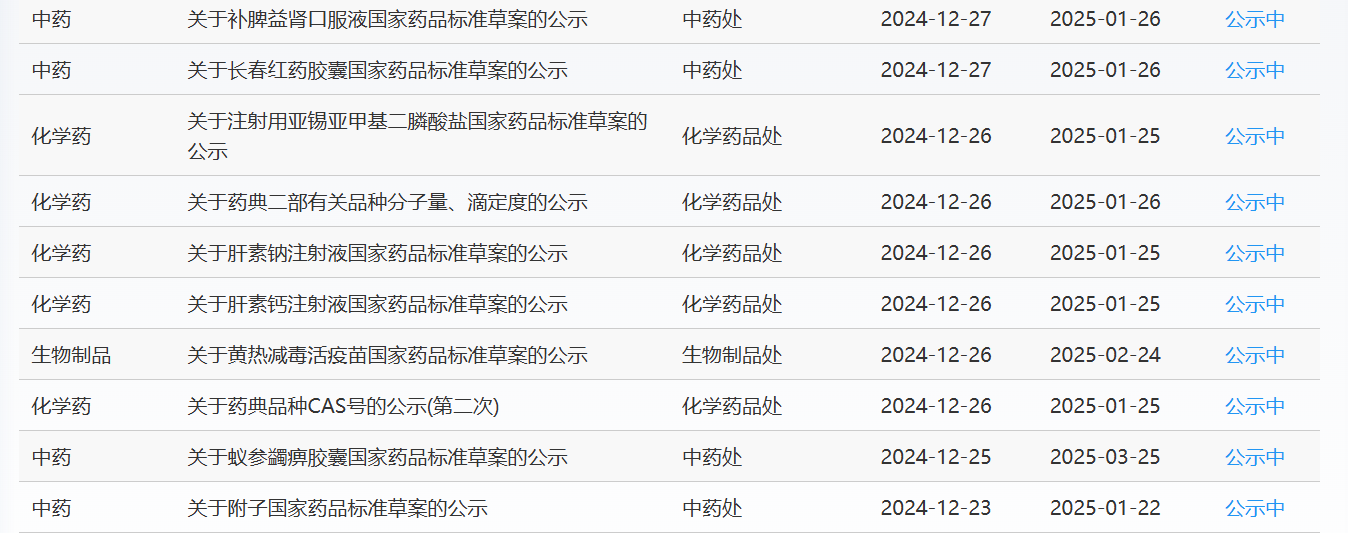

-END-


转载声明:未经本网或本网权利人授权,不得转载、摘编或利用其他方式使用上述作品。已经本网或本网权利人授权使用作品的,应在授权范围内使用,并注明“来源:新领先医药科技”。

 Hotline服务热线:010-83057670
Hotline服务热线:010-83057670
 简体中文
简体中文

 010-83057670
010-83057670 联系地址:
联系地址: 技术市场部:
技术市场部: 北京新领先
北京新领先 新领先药讯
新领先药讯 010-61006450
010-61006450
