政策法规 || 2024年度药品审评报告(附法规概览3.17-3.21)
01
2024年度药品审评报告
国家药品监督管理局药品审评中心发布2024年度药品审评报告。

扫描图中二维码
查看详细信息

02
国家药监局综合司公开征求《药品试验数据保护实施办法(试行,征求意见稿)》《药品试验数据保护工作程序(征求意见稿)》意见
为促进药品创新和仿制药发展,完善药品试验数据保护制度,根据《药品管理法实施条例》等相关规定,借鉴国际经验,国家药监局起草了《药品试验数据保护实施办法(试行,征求意见稿)》(附件1)、《药品试验数据保护工作程序(征求意见稿)》(附件2),现向社会公开征求意见。

扫描图中二维码
查看详细信息

03
关于公开征求ICH《E6(R3):药物临床试验质量管理规范技术指导原则(GCP)》原则及附件1中文翻译稿意见的通知
为推动新修订的ICH指导原则在国内的平稳落地实施,我中心组织翻译了《E6(R3):药物临床试验质量管理规范技术指导原则(GCP)》原则及附件1。现对E6(R3)原则及附件1中文翻译稿公开征求意见,为期1个月。

扫描图中二维码
查看详细信息

01
截止2025年3月21日15:00本周发布252个待领取药品批准证明文件,其中注射液59个,一致性评价品种13个。
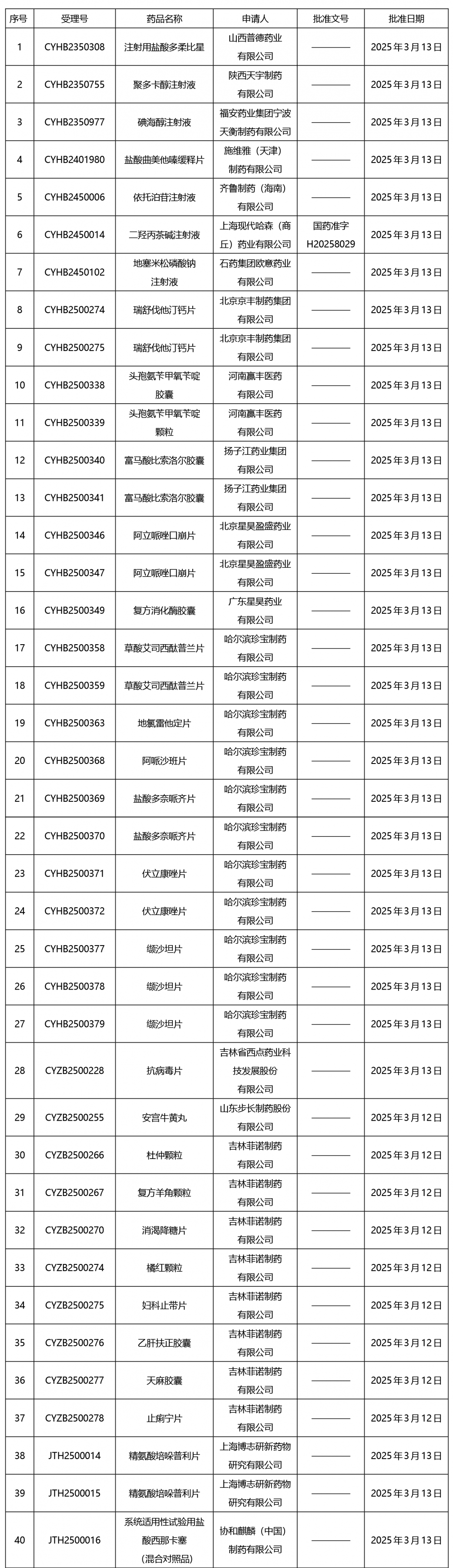
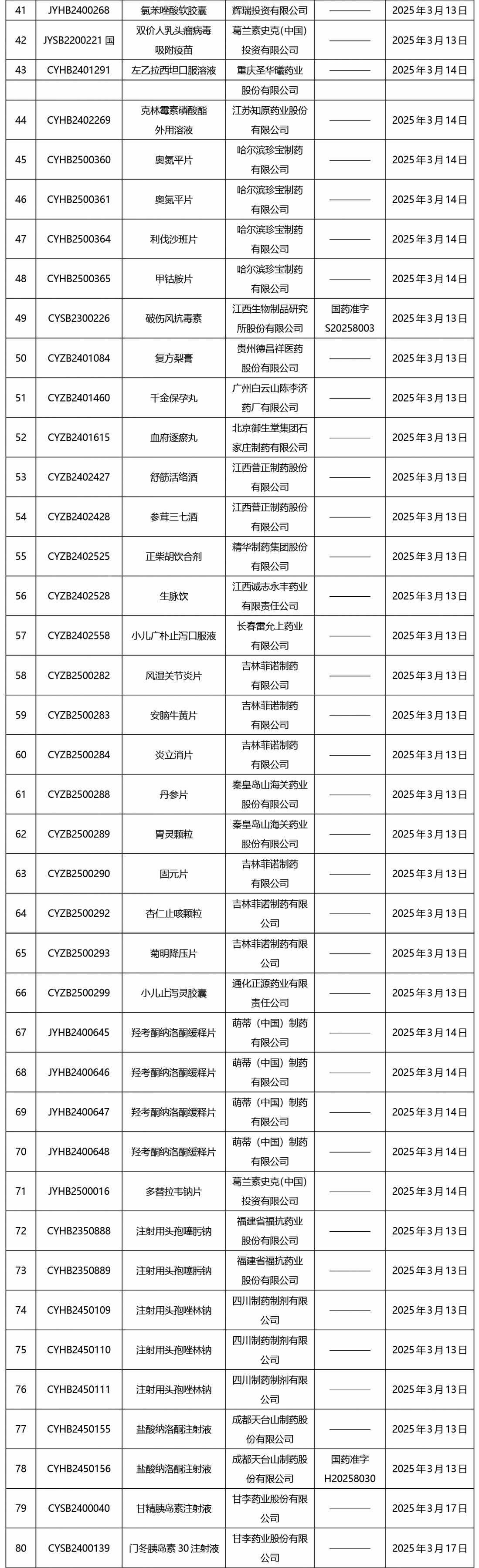
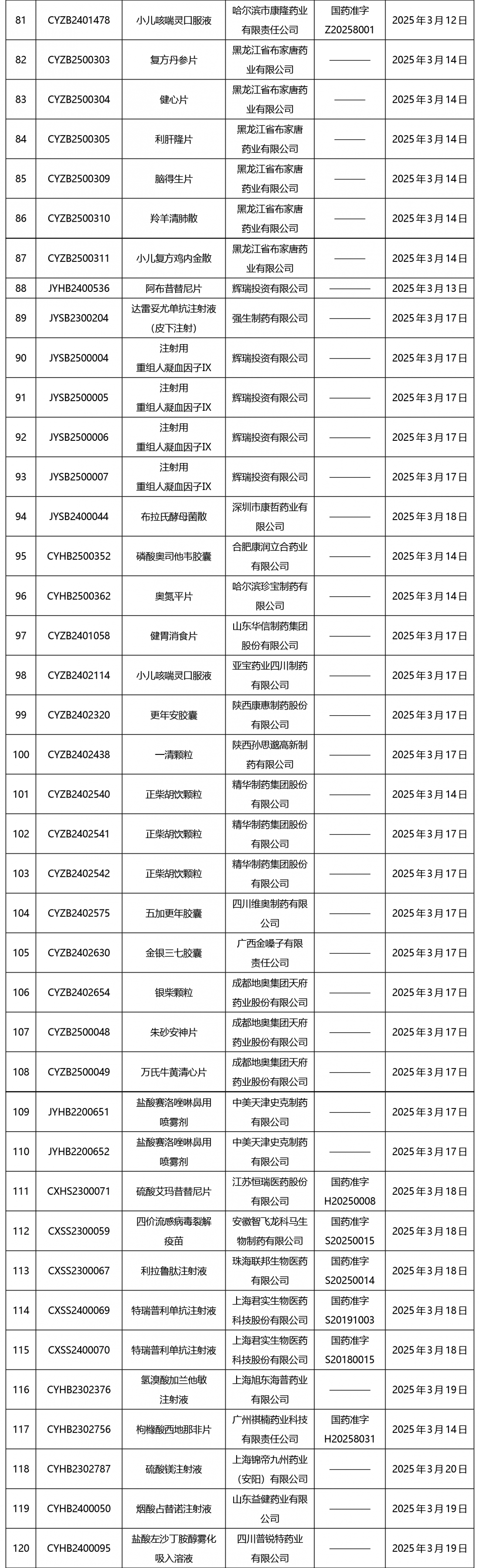
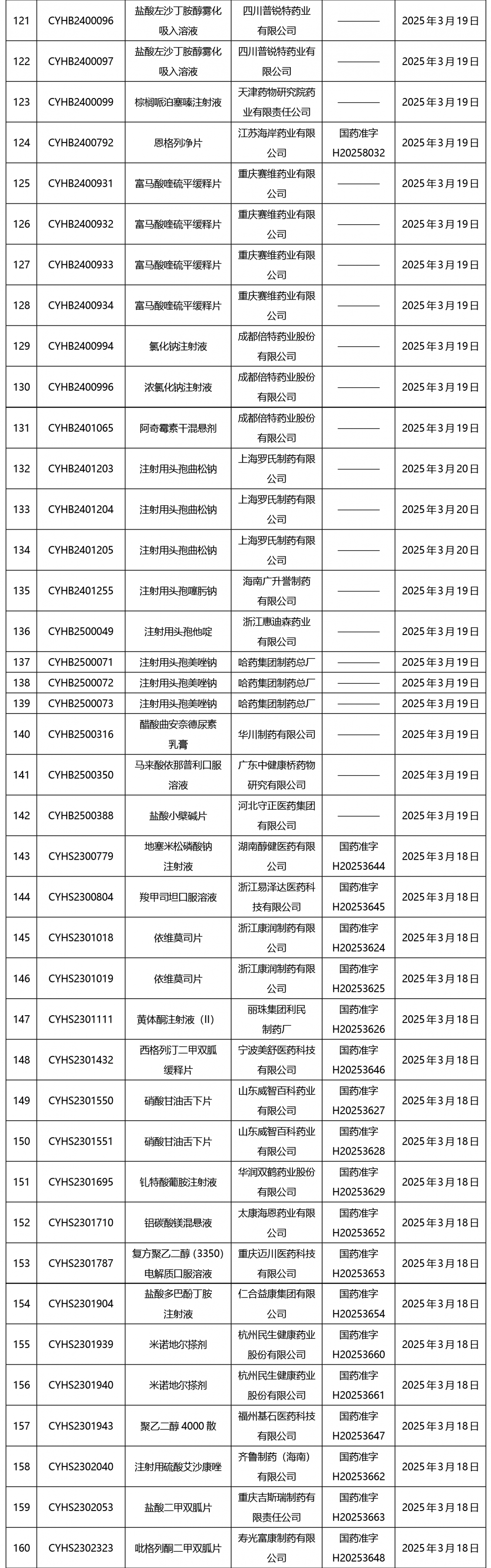
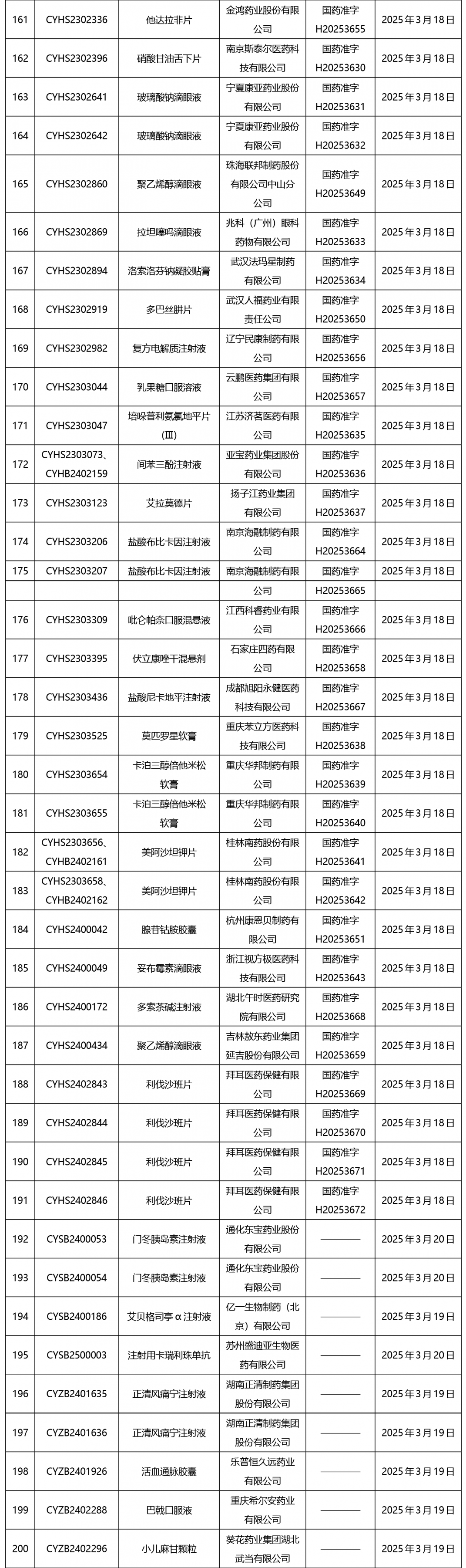
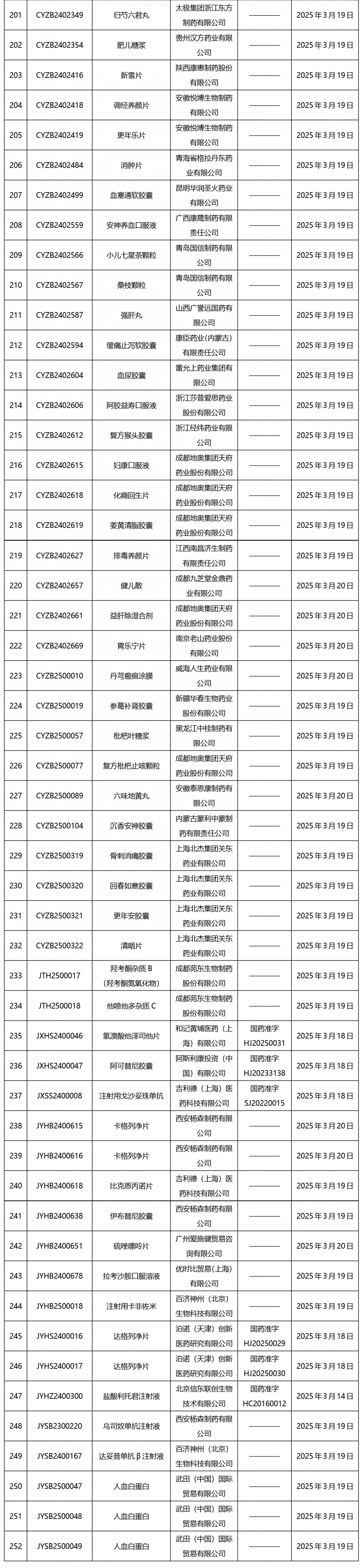
02
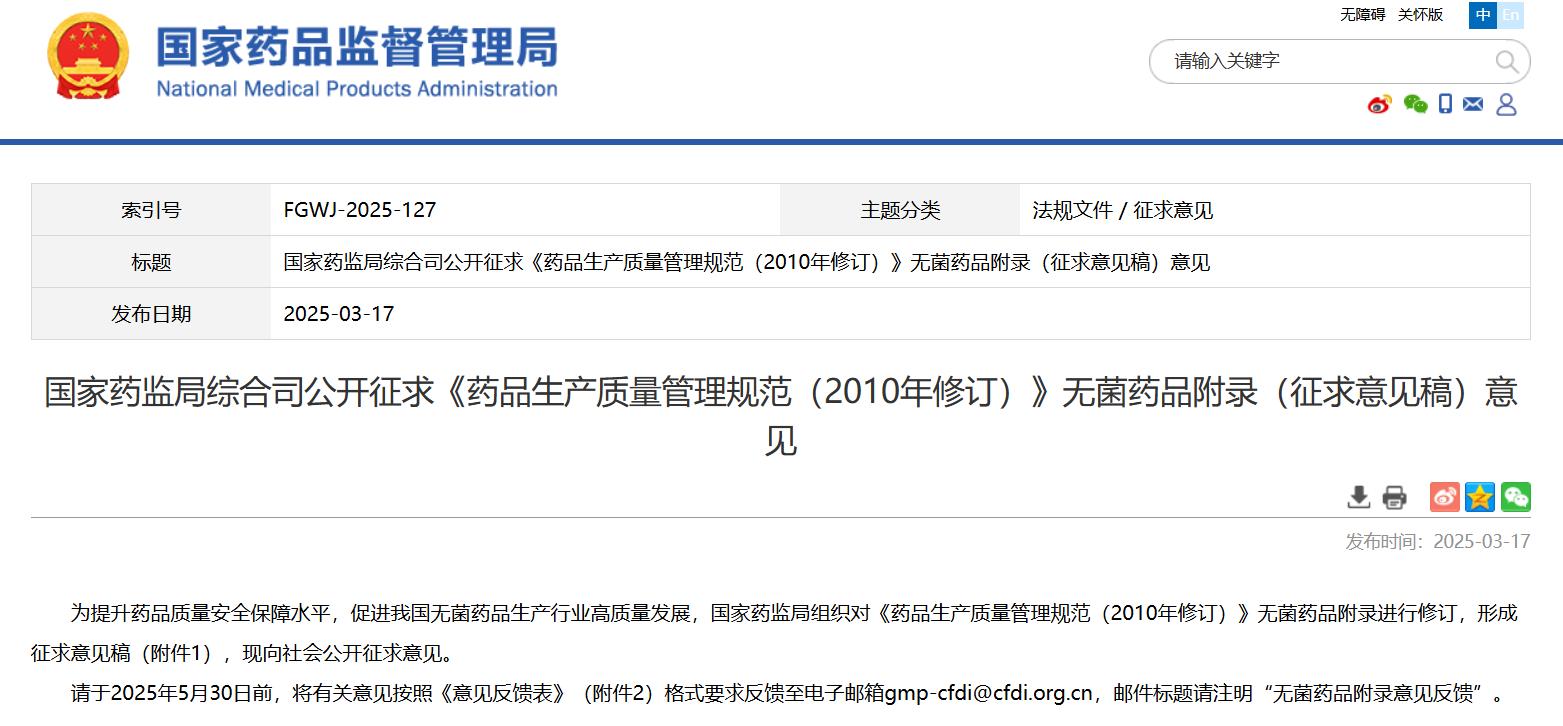
国家药监局综合司公开征求《药品生产质量管理规范(2010年修订)》无菌药品附录(征求意见稿)意见
扫描图中二维码
查看详细信息

03
国家药监局关于47批次不符合规定化妆品的通告(2025年第10号)

扫描图中二维码
查看详细信息

01
关于公开征求《化学仿制药参比制剂目录(第九十二批)》(征求意见稿)意见的通知

扫描图中二维码
查看详细信息

-END-


转载声明:未经本网或本网权利人授权,不得转载、摘编或利用其他方式使用上述作品。已经本网或本网权利人授权使用作品的,应在授权范围内使用,并注明“来源:新领先医药科技”。

 Hotline服务热线:010-83057670
Hotline服务热线:010-83057670
 简体中文
简体中文

 010-83057670
010-83057670 联系地址:
联系地址: 技术市场部:
技术市场部: 北京新领先
北京新领先 新领先药讯
新领先药讯 010-61006450
010-61006450
