政策法规 ||《化学仿制药参比制剂目录(第九十七批)》(征求意见稿)(附法规概览8.25-8.29)
01
关于公开征求《化学仿制药参比制剂目录(第九十七批)》(征求意见稿)意见的通知

点击下方链接
查看详细信息
https://www.cde.org.cn/main/news/viewInfoCommon/3bd0e121d62b5ab0555b95ac58cc47f2
02
国家药监局药审中心关于发布《化学药品仿制药上市许可申请模块二药学资料撰写要求(试行)》的通告(2025年第32号)

点击下方链接
查看详细信息
https://www.cde.org.cn/main/news/viewInfoCommon/8173832d915fc5c592ff840651f4bd38
01
本周共发布302项药品批准证明文件送达信息。
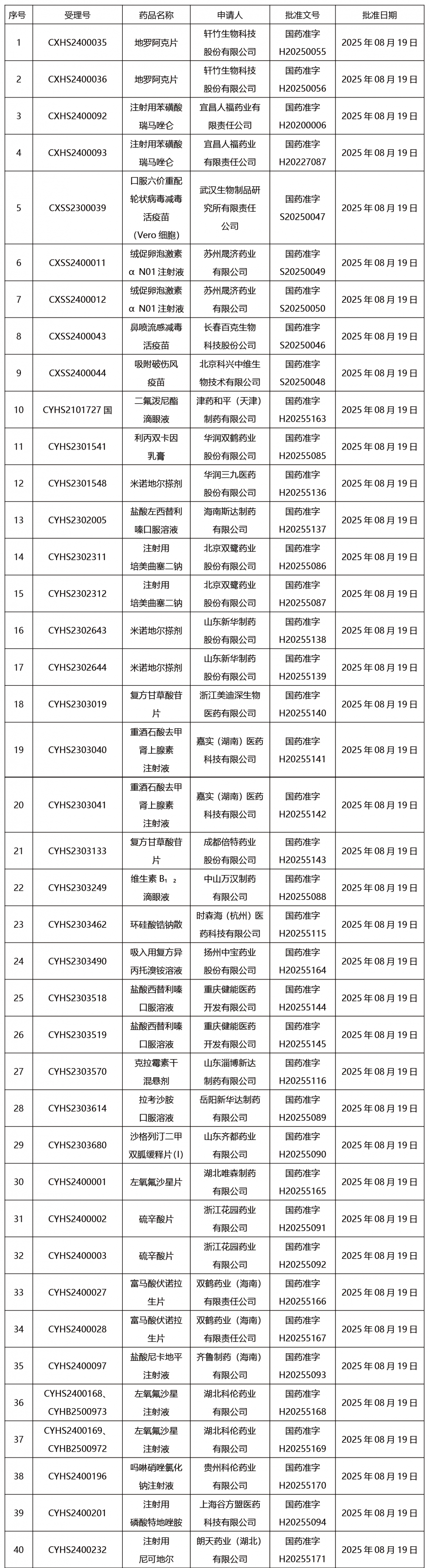
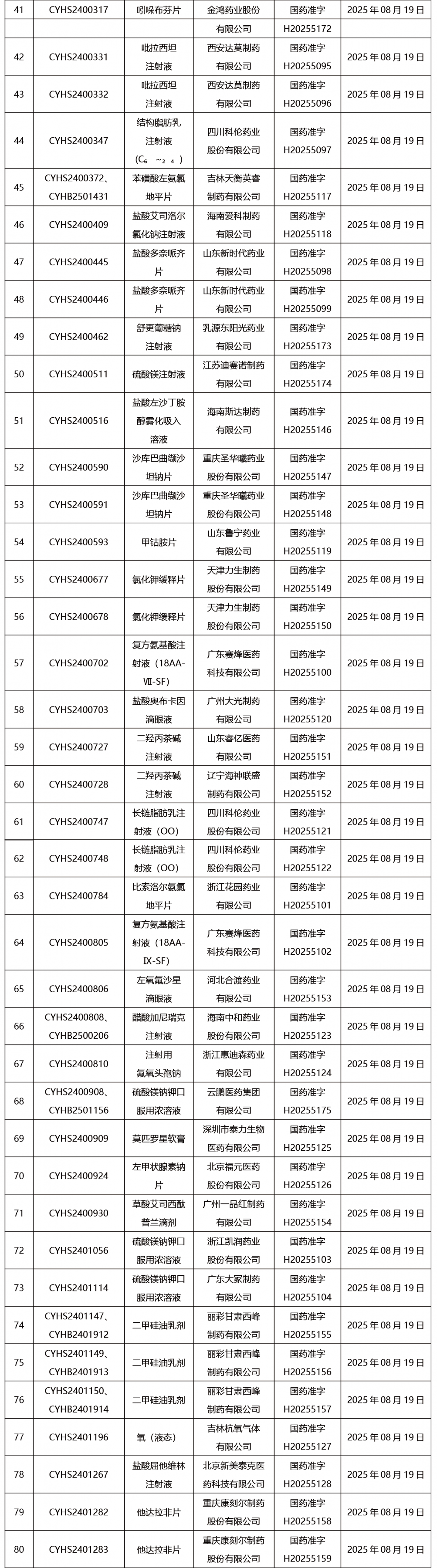
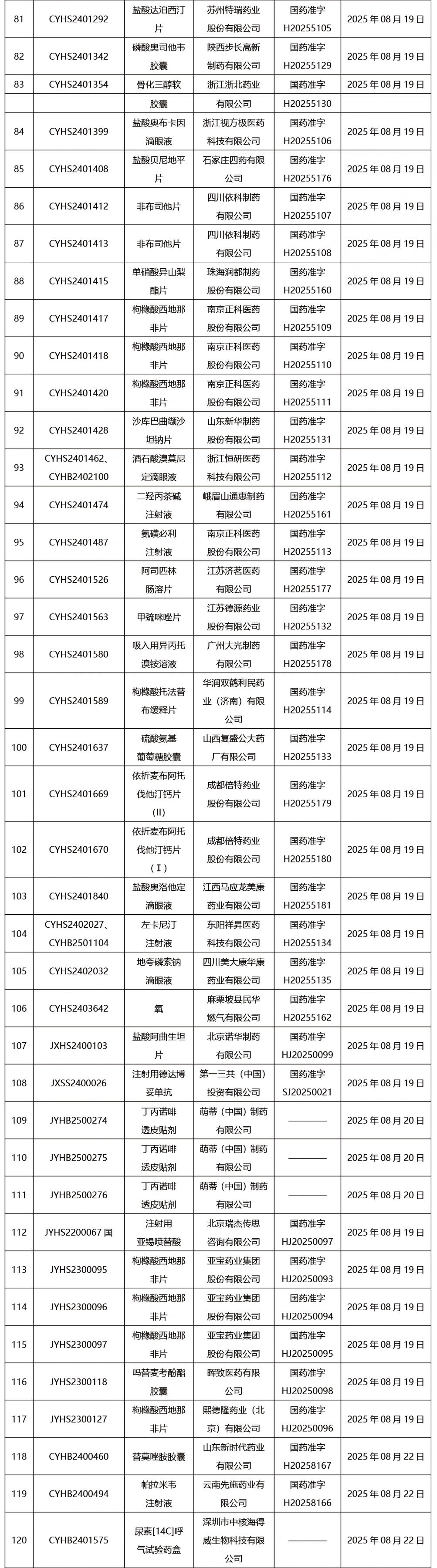
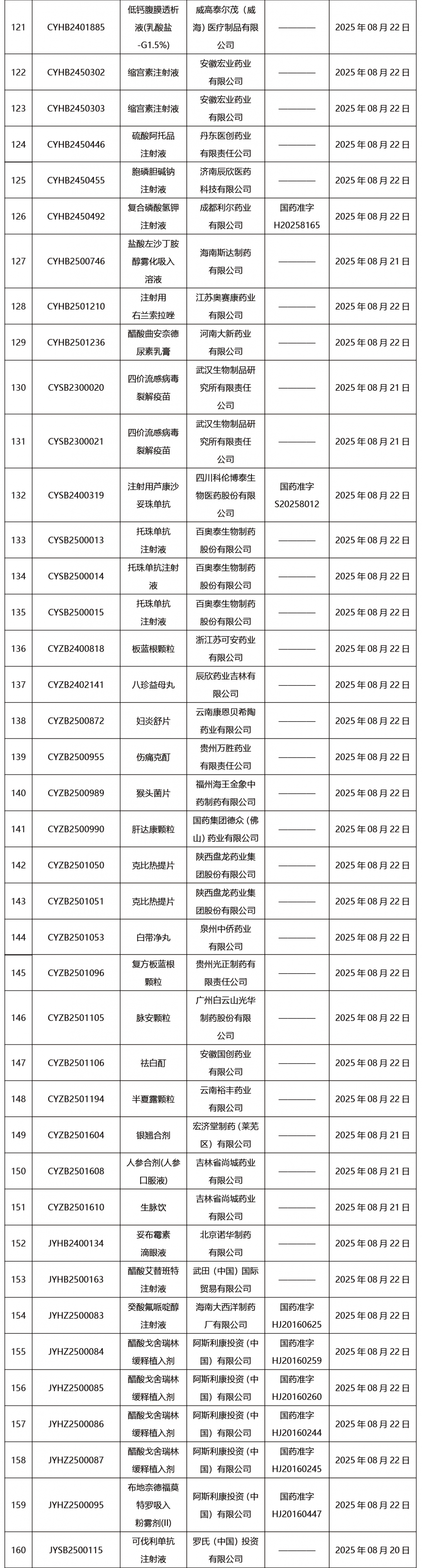
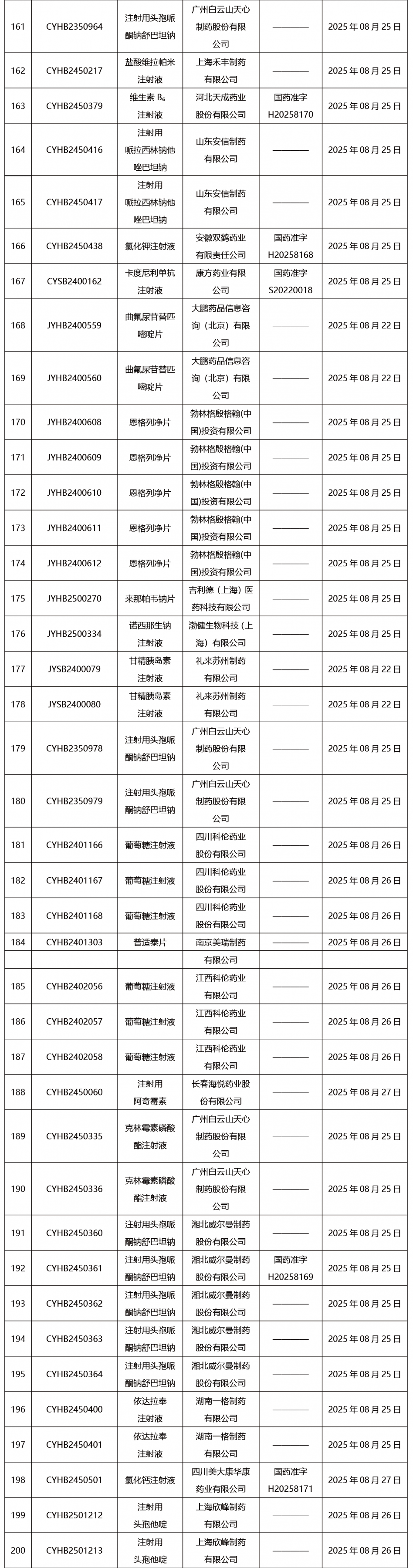
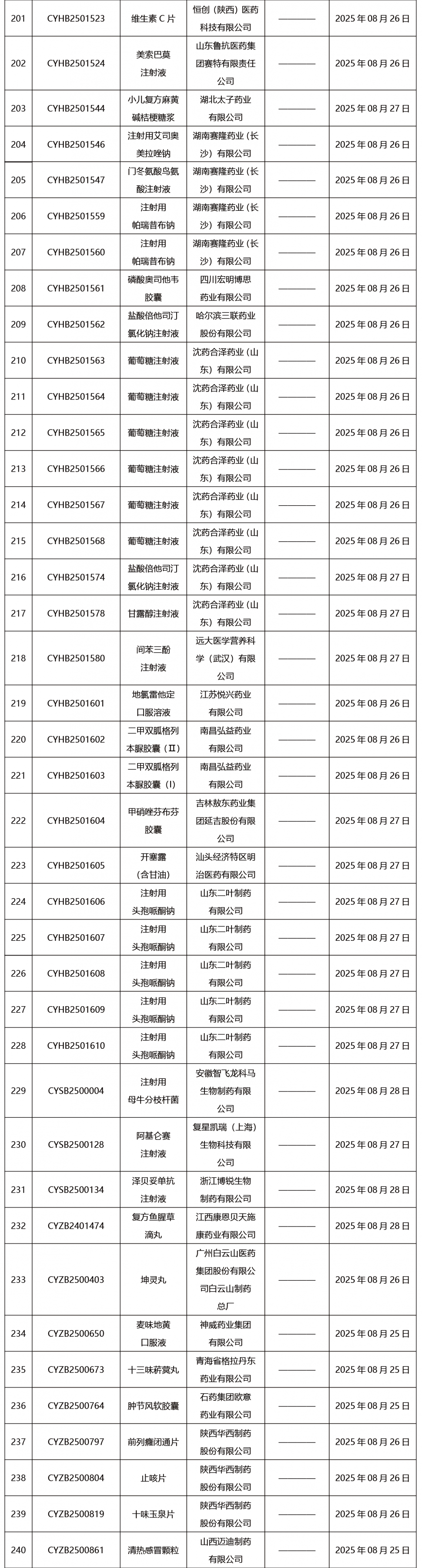
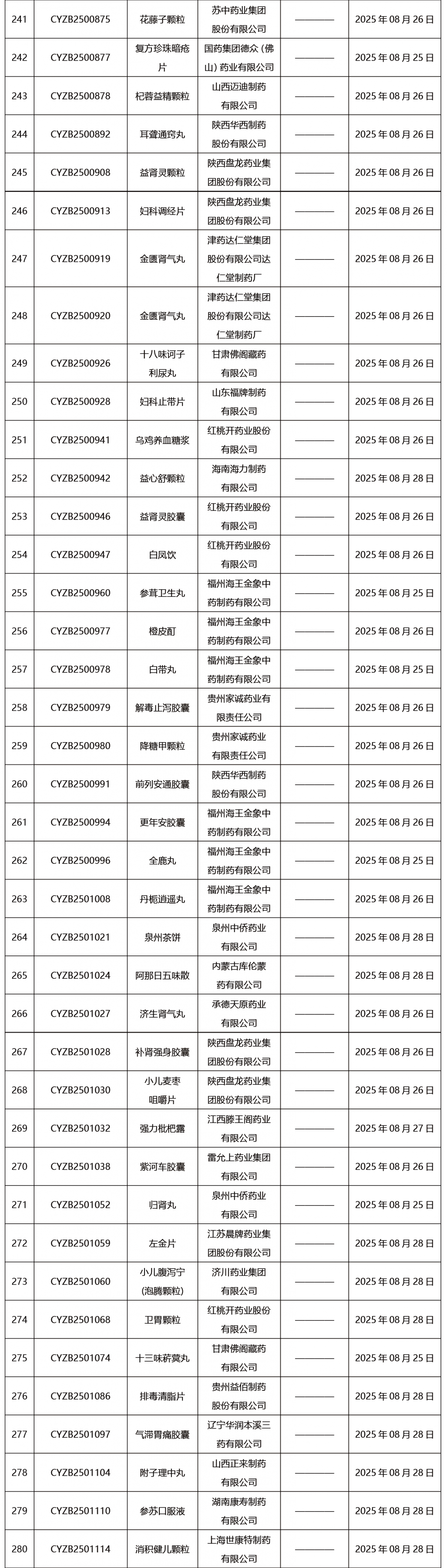
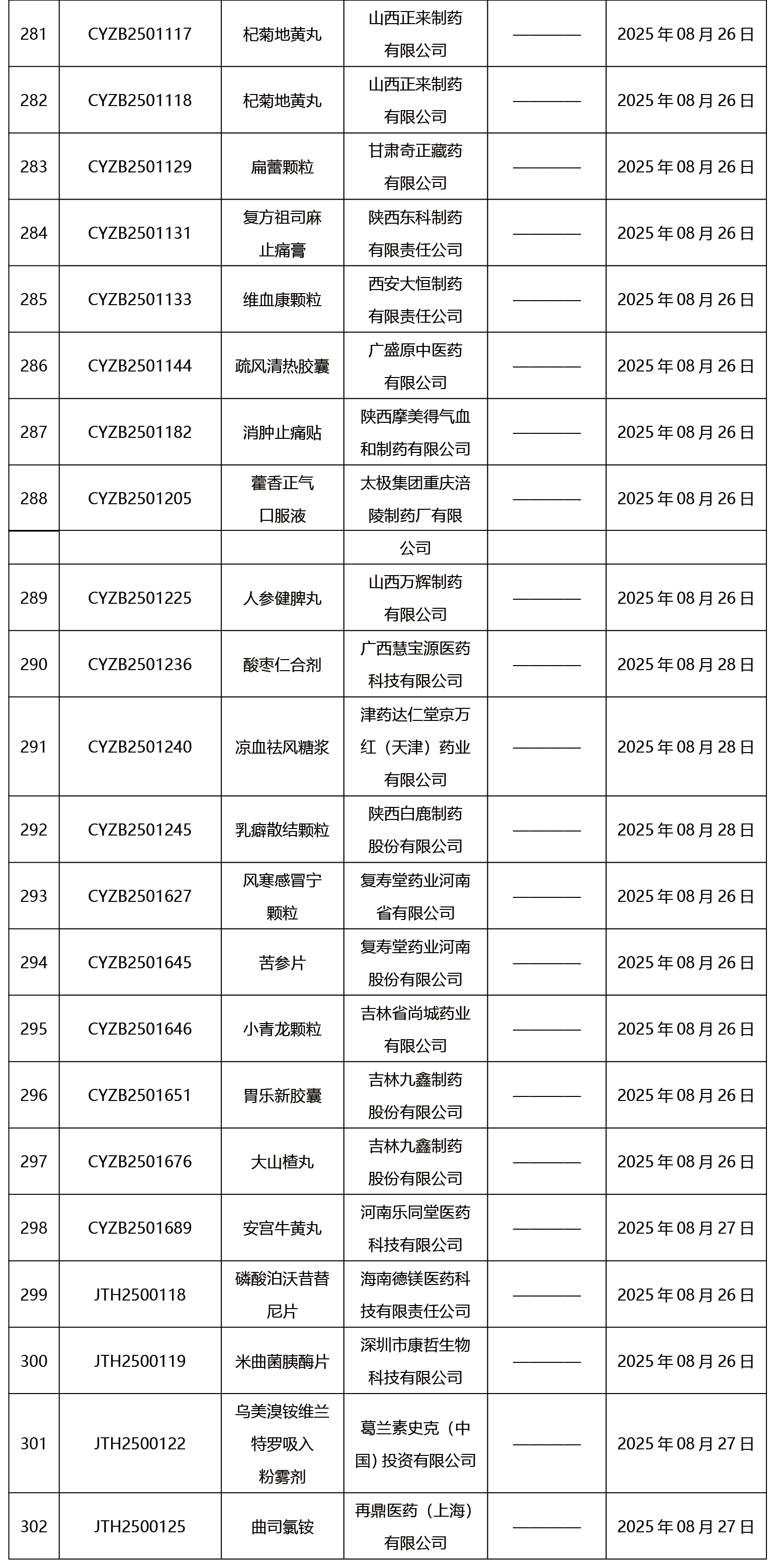
CDE
01
国家药监局药审中心关于发布《疫苗佐剂非临床研究技术指导原则》的通告(2025年第36号)

点击下方链接
查看详细信息
https://www.cde.org.cn/main/news/viewInfoCommon/886af98cc4c51bc86e8ecb816ec634c5
02
关于公开征求《预防用生物制品批准后药学变更管理方案技术指导原则(征求意见稿)》意见的通知

点击下方链接
查看详细信息
https://www.cde.org.cn/main/news/viewInfoCommon/f686913c23aedf3d126748ab13e1b9cf
03
关于公开征求ICH《E6(R3):药物临床试验质量管理规范技术指导原则(GCP)》原则及附件1实施建议意见的通知

点击下方链接
查看详细信息
https://www.cde.org.cn/main/news/viewInfoCommon/aa3e4b17f74fd27f1589fbcbb3b93f64
近期,药典委发布的标准草案公示如下:
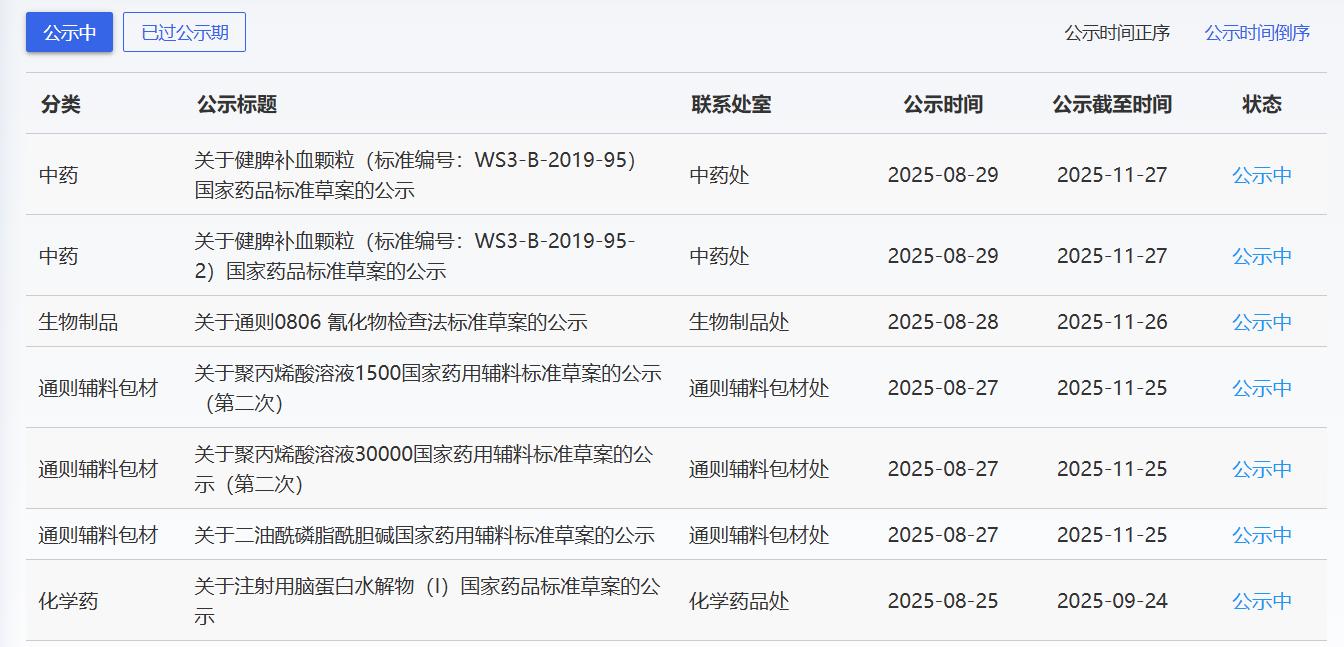
-END-


转载声明:未经本网或本网权利人授权,不得转载、摘编或利用其他方式使用上述作品。已经本网或本网权利人授权使用作品的,应在授权范围内使用,并注明“来源:新领先医药科技”。

 Hotline服务热线:010-83057670
Hotline服务热线:010-83057670
 简体中文
简体中文

 010-83057670
010-83057670 联系地址:
联系地址: 技术市场部:
技术市场部: 北京新领先
北京新领先 新领先药讯
新领先药讯 010-61006450
010-61006450
