政策法规《化学仿制药参比制剂目录(第八十批)》(征求意见稿)(附法规概览03.18-03.22)
01
关于公开征求《化学仿制药参比制剂目录(第八十批)》(征求意见稿)意见的通知
参比制剂是指用于仿制药质量和疗效一致性评价的对照药品,通常为被仿制的对象,如原研药品或国际公认的同种药物,参比制剂应为处方工艺合理、质量稳定、疗效确切的药品。经国家药品监督管理局仿制药质量和疗效一致性评价专家委员会审核确定,现发布仿制药参比制剂目录(第八十批)(征求意见稿),新增44个品规的参比名单;另外12个增加变更后上市许可持有人、增加上市许可持有人、不限定上市国及产地等。

扫描识别图中二维码
查看详细信息

02
关于公开征求ICH《Q3C(R9):杂质:残留溶剂的指导原则》实施建议和中文版意见的通知
为推动ICH指导原则在国内的平稳落地实施,国家药品监督管理局药品审评中心拟定了《Q3C(R9)指导原则实施建议》,同时组织翻译了Q3C(R9)指导原则的中文版。现对该实施建议和中文版公开征求意见。

扫描识别图中二维码
查看详细信息

01
2024年3月18日中药品种保护受理公示

扫描识别图中二维码
查看详细信息

02
国家药监局关于阿胶当归胶囊和芪参补气胶囊转换为非处方药的公告(2024年第27号)

扫描识别图中二维码
查看详细信息

03
国家药监局关于修订复方金银花颗粒和普乐安制剂说明书的公告(2024年第28号)
扫描识别图中二维码
查看详细信息

04
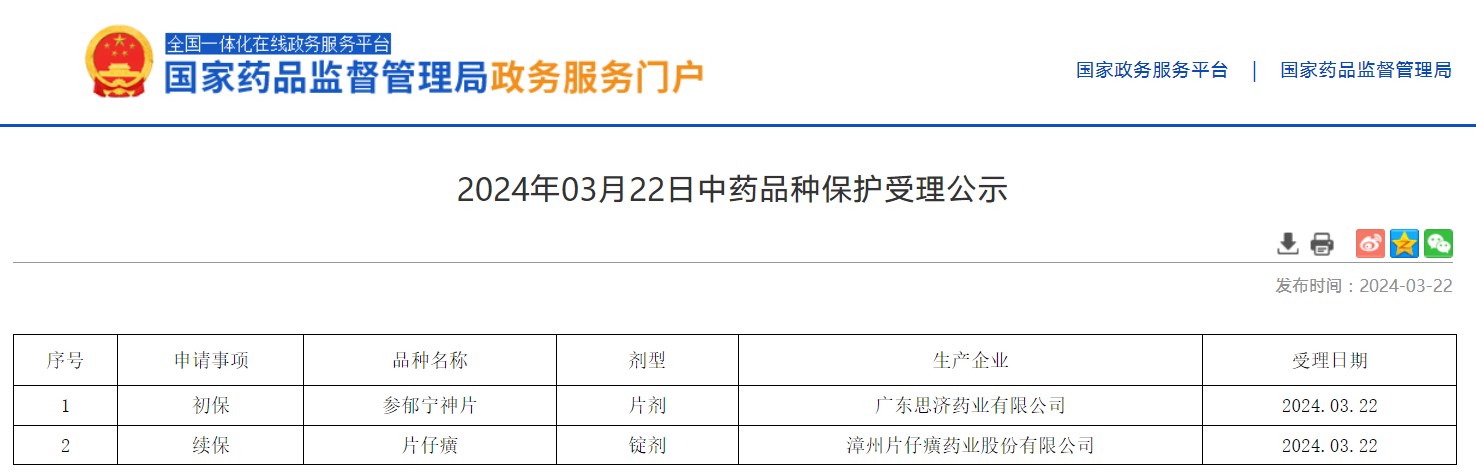
2024年03月22日中药品种保护受理公示
扫描识别图中二维码
查看详细信息

01
关于做好2024年度国家药品标准提高工作的通知
扫描识别图中二维码
查看详细信息

02
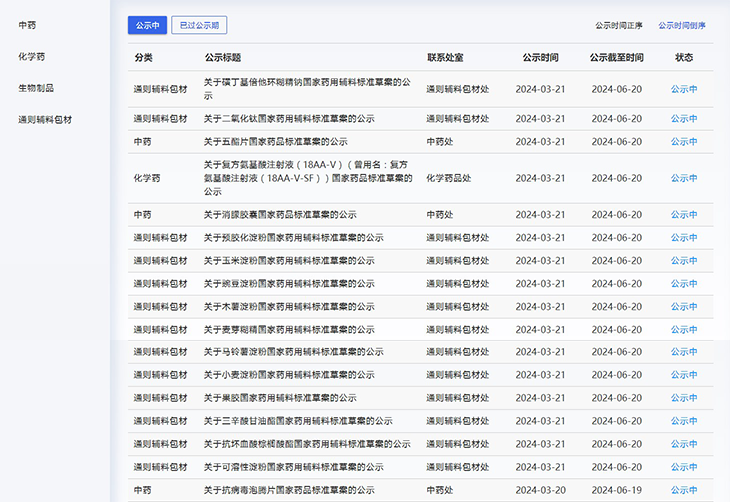
本周,药典委发布的药品及药用辅料标准草案如下
扫描识别图中二维码
查看详细信息

-END-


转载声明:未经本网或本网权利人授权,不得转载、摘编或利用其他方式使用上述作品。已经本网或本网权利人授权使用作品的,应在授权范围内使用,并注明“来源:新领先医药科技”。

 Hotline服务热线:010-83057670
Hotline服务热线:010-83057670
 简体中文
简体中文

 010-83057670
010-83057670 联系地址:
联系地址: 技术市场部:
技术市场部: 北京新领先
北京新领先 新领先药讯
新领先药讯 010-61006450
010-61006450
