口服固体常释制剂研发工艺技术要点解析(上)
目前,在全球制药产业链结构中,创新药一直是医药企业发展的主角,但不可否认,仿制药是世界需求的主体,也是我国目前生产的主要方向及临床用药的主体,仿制药的质量与公众用药的安全性和有效性息息相关。 截至2020年,我国有17万个药品批准证明文件,其中包括化学药批文10.7万个。目前我国超过5000家制药企业,生产的药品95%以上是仿制药,是一个名副其实的仿制药大国。
近年来,为了提高国产仿制药的质量,促进医药产业的结构调整和升级,我国政府已经出台了一系列的政策来推进仿制药质量与疗效的一致性评价顺利开展。在仿制药开发及一致性评价研究过程中,有几个口服固体常释制剂研发工艺技术要点想和大家分享下,以期将这项工作做好,不足之处,欢迎批评指正。本文所述口服固体制剂单指常规释放口服固体制剂,不包括缓释、控释及其它特殊固体制剂。
口服固体制剂研发工艺技术要点
口服固体制剂研发工艺技术要点主要分为固体制剂的基本质量属性、溶出特性、稳定性以及均匀性四大方面。本文将对各个方面结合所开展项目进行以下讨论。
固体制剂的基本质量属性
固体制剂包含了片剂、硬胶囊剂、颗粒剂、干混悬剂等诸多剂型仿制药首先要做到基本质量属性符合ICH和各国药典的要求。 在仿制药一致性评价项目开发过程中,诸多项目由于基本质量属性不过关,或在工业设备上存在形形色色的问题,延长项目开发周期,在抢占市场上处于劣势。
本文所述固体制剂基本质量属性包括诸如片剂可压性(硬度范围、压片速度范围、是否裂片、是否粘冲、片面光泽程度);片剂剂量均匀性;硬胶囊剂的装量差异、生产设备的填充速度范围;颗粒剂及干混悬剂的粒度、水分;小规格制剂的含量均匀度等等。
在项目的开发中,我们发现片剂的可压性在很多时候影响了项目进度,也是工业化生产经常出现问题的地方。本文对于这个问题进行了细致分析,以期对这类问题有一个规律性的认识。
❖项目A—主药含量占比75%的普通片剂
✎问题:在工业化生产阶段个别批次压片存在顶裂,不顶裂批次素片在包衣过程中,片剂划痕严重。
✎诊断:API为弹性物料,片剂可压性存在问题。
✎解决:总体思路,通过处方及制备工艺的改进,增加片剂可压性(含素片耐磨性),细化包衣参数,保证包衣过程不出现划痕及黏连。
具体措施包括:
a. 调整API粒径控制范围;
b. 调整粘合剂处方占比;
c. 更换影响片剂可压性的关键辅料预胶化淀粉的来源;
d. 改进湿法制粒工艺,控制中间体颗粒粒度分布,细化包衣参数,保证在包衣初始阶段片剂片面不出现划痕。
✎解读:片剂可压性不好,存在于很多API占处方比例较大的项目中,而API如果为弹性物料(尤其是显微状态下为棒状或片状形态),则项目在工业化设备高速压片时大概率会存在可压性问题,如裂片。裂片的机理为片剂内部结合力不足以抵消物料颗粒的弹性复原率。要消除物料弹性复原率,可以减小弹性物料的粒径。辅料方面需要选择可压性较好的辅料,同时控制压片前中间体颗粒的粒度分布及水分;工业生产用高速压片机压片速度较快,要保证一定生产效率,物料的性质要做到最优。
项目A原料药粒径范围对可压性考察结果
❖ 项目B —主药含量占比15%的普通片剂,片面存在刻痕,顶喷制粒工艺,外混辅料
✎问题:在工业化生产阶段压片存在粘冲,压片过程中存在含量分层,前中后素片含量差异超过5%。
✎诊断:顶喷制粒后颗粒粒度分布不均匀,细粉占比较大; 外混辅料选择型号不合适。
✎解决:
① 通过调整顶喷制粒工艺参数,来改善制粒后颗粒粒度分布,使颗粒粒度分布更加均匀;
② 外混微晶纤维素选择直压型号,并且关注微晶纤维素粒度与顶喷制粒后的颗粒粒度与堆密度,在压片过程中注意供料转速与压片速度相匹配。
✎解读:片剂粘冲大部分情况下为压片前中间体颗粒细粉占比较多,可压性辅料占处方比例或型号选择不合适。
片剂粘冲的本质是因为片剂表面物质之间的结合力小于片剂表面与冲头的结合力,多发生于片剂刻痕或logo处,在排除设备因素、压片速度、颗粒水分的前提下,粉体的粒度分布尤其是颗粒细粉的比例非常关键;
压片前中后含量的差异较大,很大程度上也是由于颗粒粒度分布不均匀造成的,如果处方中有较多占比的外混辅料,则工艺开发中需要保持外混辅料与所制颗粒粒度分布接近,堆密度接近,颗粒形态最好也接近。
小结:由上述两个例子可以看出,影响固体制剂基本质量属性的因素主要有两个方面,处方方面和制备工艺参数方面。
1、在进行仿制药的开发中,如果限定了辅料的种类或型号,就要考虑制备工艺参数的调整;
2、在某些情况下,由于国内制剂设备性能的局限,制备工艺参数调整的余地较小时,要重点关注辅料的型号及其作用。
固体制剂的溶出特性
固体制剂仿制药开发过程中,溶出特性是一个重点和难点。有诸多文献和指导原则对仿制药和参比制剂的溶出一致性做了论述,尤其是谢沐风老师的系列文章对此做了深刻的剖析解读。本文重点从处方及制备工艺角度说明仿制药如何做到与参比制剂溶出相似,降低体内生物等效风险。
参比制剂的溶出特性的解读:仿制药溶出特性的研究起点是从剖析参比制剂的溶出特性开始的。参比制剂溶出特性剖析的关键在于:① 具有区分力溶出条件的选择;② 参比制剂溶出现象的解读。参比制剂的溶出特性剖析需要结合理解参比制剂设计的初衷及API特有的理化性质(如pKa)。
具有区分力溶出条件的选择,如有药典标准,需要比较各国药典标准溶出度方法的区分力; 同时可以结合API在各pH条件下溶解度及API pKa值选择其它可能有区分力的介质; 降低转速以期获得区分力介质也不失为个好办法。
本公司依靠体内外中心Hemanth博士建立体外溶出与体内药代动力学的预测模型来指导仿制药的开发,在参比制剂多条介质溶出曲线剖析完成后,通过预测模型确定哪条关键介质溶出曲线或哪几条关键介质溶出曲线为表征体内外关系的特征溶出曲线,提高了预BE、BE的通过率,从而提高了仿制药开发的效率。
参比制剂溶出现象及溶出数据的解读,在参比制剂溶出特性剖析时,首先应重视溶出现象的观察与思考,溶出现象大致分为两类,崩散性与溶蚀性。包衣片应关注包衣脱落时间,胶囊剂应关注胶囊壳破裂时间,颗粒剂及干混悬剂应关注颗粒分散状态,如颗粒加入溶出杯中是否有漂浮,是否有聚集 。
❖项目C —复方普通片剂 ,a主药为难溶性成分,b主药为易溶性成分,参比制剂制备工艺为两成分分别制粒,两种颗粒混合,外加辅料压片。参比制剂溶出现象为崩散型。
✎问题:参比制剂a成分拟合溶出曲线(缓慢溶出),b成分极快速溶出(5min溶出90%以上),仿制制剂保证a成分和b成分均与参比制剂拟合。
✎诊断:参比制剂溶出现象为崩散型,并且两种主药成分颗粒混合后压片,b成分为极快速溶出,a成分为缓慢溶出,即崩散后两种主药各自从两部分颗粒中溶出。
✎解决:首先保证崩散时间与参比制剂基本一致,本项目仿制制剂外混辅料含微晶纤维素,并无专门崩解剂即可保证崩散时间。a成分颗粒的处方经过充分的筛选最后确定API的粒径对a成分的溶出特性影响最为关键、粘合剂型号次关键、制粒工艺影响更次之(但制粒工艺影响a成分颗粒的粒度分布,从而影响两种成分的混合均匀度及压片的含量分层风险,详细分析在本文2、4部分介绍)。
✎解读:口服固体制剂溶出特性基本从三个方面考虑API理化性质:
① 粒径是个很关键的因素,尤其对于难溶性药物;
② 处方占比最大的辅料型号及用量也是非常关键的因素,制备工艺对于崩散性制剂影响有限,但是很多情况下会影响溶蚀性制剂溶出特性;
③ 在复方制剂中,如主成分分别制粒,则两部分颗粒的颗粒性质(粒度分布及堆密度)对产品的溶出特性影响关键。仔细观察参比制剂的溶出现象并分析原因是仿制药开发需要重视的内容。
小结:研究仿制药的溶出特性,应与药物的体内药代动力学联系起来,要思考为什么参比制剂会有剖析得到的溶出特性,而非简单的为了拟合溶出而拟合。具体内容可参见新领先药讯《体内外相关性研究在口服固体制剂仿制药过程中的应用》。
由于文章篇幅所限,关于稳定性和均匀性的相关解读,详见下期《口服固体常释制剂研发工艺技术要点解析(下)》。
-END-
关于我们:
固体制剂事业部做为公司核心板块之一,致力并搭建药物缓释、控释、靶向制剂及微囊、固体分散体、包合、速溶技术、难溶性药物等多项制剂技术平台,在多领域药物研发积累了丰富经验。
固体制剂事业部目前在研项目50余个,每年能够完成近20个项目的申报,开发品种涉及片剂、胶囊剂、颗粒剂等多个剂型,覆盖心脑血管用药、抗肿瘤、抗生素、老年性疾病用药、消化系统等多个领域。
公司拥有雄厚的固体制剂药品研发实力,丰富的资源:
· 专家顾问团队,由业内知名专家组成,对NMPA政策法规解读深入,协助合理把控项目,技术支持到位;
· 体内外桥接团队,由资深国际化药剂学科学家领导,以临床目标指导制剂开发,降低BE风险;
· 制剂开发团队,制剂开发经验丰富,配置数百平米的专业实验室,国内外先进制剂设备,可实现片剂、胶囊剂、颗粒剂等多剂型产品的制备及检测;
· 产业化团队,具有丰富的工厂生产经验及实验室研究经验,为实现制剂由实验室研究转化为工厂规模化生产保驾护航;
· 中试车间,拥有GMP认证的制剂中试车间,为高质量的新药研究提供基础保障。
我公司为客户提供以产业化为核心的具有全球化技术水准的药学技术服务,为让中国新药技术和生产工艺与世界同步而努力。
转载声明:未经本网或本网权利人授权,不得转载、摘编或利用其他方式使用上述作品。已经本网或本网权利人授权使用作品的,应在授权范围内使用,并注明“来源:新领先医药科技”。

 Hotline服务热线:010-61006450
Hotline服务热线:010-61006450
 简体中文
简体中文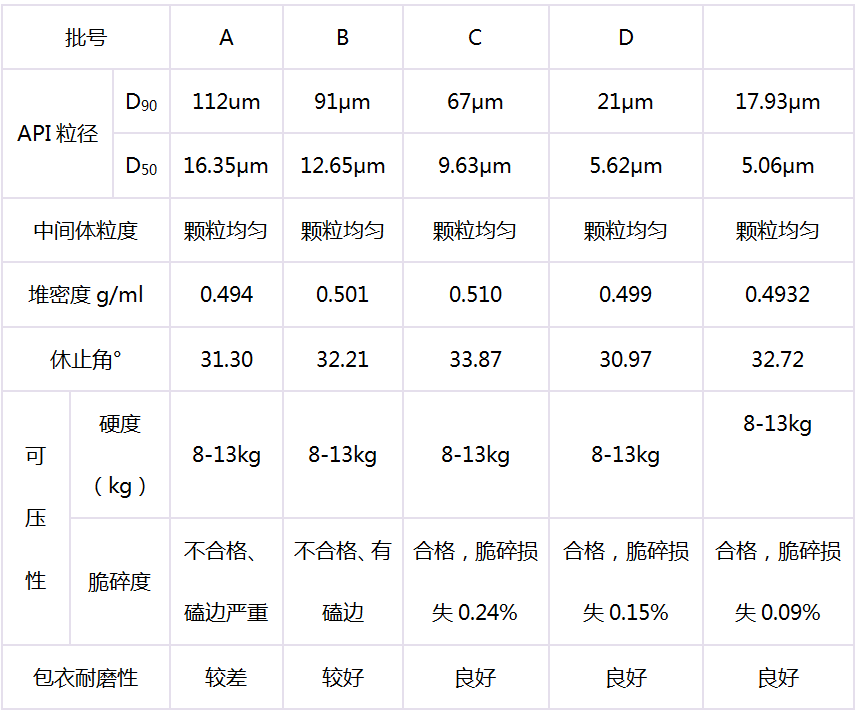



 010-61006450
010-61006450 联系地址:
联系地址: 技术市场部:
技术市场部: 北京新领先
北京新领先 新领先药讯
新领先药讯 010-61006450
010-61006450
